ENERO 2022
Caso enviado por los Dres. C. Izurieta, E. Pueo, D. Viles, M. Zielonka, I. Hernández, F. Worner. Hospital Universitario Arnau de Vilanova, Lleida, España.
Presentamos el caso de una mujer de 60 años, HTA, DLP y con cardiopatía isquémica crónica.
Algunos de sus antecedentes aportados fueron:
2007 ECG con necrosis inferior.
• ETT: FEVI 40 – 45%, aquinesia inferior e inferolateral e IM moderada a severa (funcional).
• ETE: VM estructuralmente normal con IM moderada y FOP.
• SPECT: FEVI 33%, necrosis inferior.
• CRG: DA sin lesiones, Dx de pequeño calibre con lesión severa, ausencia de Cx, CD dominante sin lesiones.
2017 (otro país): diagnóstico de IM severa por prolapso de ambos velos por rotura de cuerdas y FEVI 38%.
Por lo anterior, se realizó en el año 2017 RVM con bioprótesis Perimount 27 mm + cierre de FOP.
La elección de la bioprótesis fue por negativa de la paciente a la anticoagulación.
Desconocemos datos del postoperatorio inmediato.
Actualmente, 4 años después, consulta por disnea en CF II/IV NYHA.
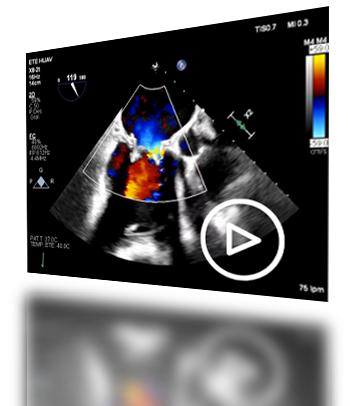
Videos 1 y 2 Desde Ecocardiograma transtorácico (4 años post cirugía) se observa un VI ligeramente dilatado, globuloso, con aquinesia del territorio basal y medio inferolateral e inferoseptal y una bioprótesis mitral severamente disfuncionante con flujo regurgitante protésico significativo y flujo diastólico con un área de convergencia proximal prominente de gran aceleración. Se intuye una doble lesión protésica al menos moderada por Doppler color.
En plano apical 4 cámaras se aprecia la bioprótesis desestructurada y con signos de calcificación. El movimiento de los velos impresiona significativamente restringido, visualizándose en este cine sólo el movimiento de uno de ellos. Existe un deterioro (cualitativo al menos) leve de la FEVI, la AI está severamente dilatada y las cavidades derechas aparentan tener tamaño y dinámica conservadas.
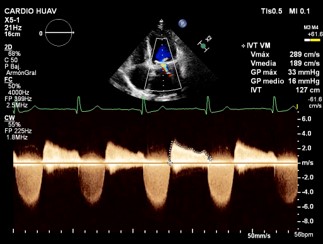
Videos 1 y 2 En las imágenes de eje largo apical se observan alteraciones degenerativas estructurales de la bioprótesis, con severa disfunción de apertura y cierre. No parece existir fuga periprotésica evidente. Con el Doppler continuo se evidencia que tanto el espectro del jet regurgitante y el flujo de entrada transvalvular son densos y bien definidos. El gradiente medio anterógrado alcanza los 16 mmHg. Se debe tener en cuenta que puede encontrarse magnificado por la severidad de la insuficiencia. Se procede a la realización del Ecocardiograma transesofágico (ETE) para mejor visualización de la prótesis.
Imagen En las imágenes de eje largo apical se observan alteraciones degenerativas estructurales de la bioprótesis, con severa disfunción de apertura y cierre. No parece existir fuga periprotésica evidente. Con el Doppler continuo se evidencia que tanto el espectro del jet regurgitante y el flujo de entrada transvalvular son densos y bien definidos. El gradiente medio anterógrado alcanza los 16 mmHg. Se debe tener en cuenta que puede encontrarse magnificado por la severidad de la insuficiencia. Se procede a la realización del Ecocardiograma transesofágico (ETE) para mejor visualización de la prótesis.
Videos 1 y 2 (de 3) Vistas de ETE en 4, 2 y 3 cámaras en esófago medio. En cuanto a la prótesis mitral, el anillo protésico aparenta conservado, radicando el problema a nivel de los velos, que se encuentran fibrosados, retraídos y engrosados. La movilidad de al menos 2 de ellos está muy restringida; en particular la del velo posterior, que impresiona fijo. No se observan imágenes compatibles con vegetación o trombo, por lo que se sospecha un extenso proceso de degeneración estructural protésico.
Video 3/3 Vistas de ETE en 4, 2 y 3 cámaras en esófago medio. En cuanto a la prótesis mitral, el anillo protésico aparenta conservado, radicando el problema a nivel de los velos, que se encuentran fibrosados, retraídos y engrosados. La movilidad de al menos 2 de ellos está muy restringida; en particular la del velo posterior, que impresiona fijo. No se observan imágenes compatibles con vegetación o trombo, por lo que se sospecha un extenso proceso de degeneración estructural protésico.
Videos 1 y 2 (de 3) En estas imágenes de ETE 2D color se aprecia la severa disfunción protésica. A 119º y a 142º en esofago medio vemos un jet regurgitante transprotésico que impresiona de grado severo. En el plano de 2 cámaras a 70º se observa un aliasing diastólico con gran aceleración proximal que genera un área de convergencia de flujo muy prominente. Durante la sístole llama la atención un pequeño flujo regurgitante, diferente al previamente descrito, que parece originarse a nivel del velo posterior internamente al anillo, correspondiente a pequeña fuga paraprotésica posterior.
Video 3/3 En estas imágenes de ETE 2D color se aprecia la severa disfunción protésica. A 119º y a 142º en esofago medio vemos un jet regurgitante transprotésico que impresiona de grado severo. En el plano de 2 cámaras a 70º se observa un aliasing diastólico con gran aceleración proximal que genera un área de convergencia de flujo muy prominente. Durante la sístole llama la atención un pequeño flujo regurgitante, diferente al previamente descrito, que parece originarse a nivel del velo posterior internamente al anillo, correspondiente a pequeña fuga paraprotésica posterior.
Video 1 y 2 En la vista quirúrgica de ETE 3D se observa el anillo protésico correctamente implantado, sin evidencia de dehiscencia. Los velos muestran una extensa degeneración con esclerosis, retracción y fusión. En su zona de implantación, especialmente a nivel del velo posteromedial, se observan masas ecogénicas, homogéneas y protruyentes, que limitan sensiblemente su movimiento. El 3D color muestra un jet regurgitante de gran magnitud.
Hallazgos descritos desde otra perspectiva, también en vista auricular. Aquí se puede observar el velo posteromedial, (situado arriba), internamente al anillo, el área de mayor engrosamiento y protrusión.
Vista ventricular de la bioprótesis que muestra las 3 astas de inserción y la impronta del anillo sin anomalías. Los velos se encuentran engrosados, con signos de retracción, fusión y restricción parcial de su movilidad, siendo total la del velo posteromedial (velo en posición superior derecha en la imagen). La apertura valvular está muy limitada.
Vista ventricular 3D de la bioprótesis con angulación modificada respecto a la anterior. Observamos que la apertura de los velos está limitada. Llama la atención una solución de continuidad en la base del velo posteromedial (en posición superior-derecha en la imagen), que podría corresponder a perforación del mismo.
Visión ventricular 3D color de la bioprótesis que muestra claramente el flujo sisto-diastólico de gran aceleración tanto transvalvular central como a través de la perforación del velo posterior.
La planimetría 3D (por MPR) del área valvular mitral es de 0.9 cm2, compatible con una estenosis significativa (si bien no existen puntos de corte establecidos para definir el grado de severidad de la estenosis protésica, extrapolamos el valor utilizado sobre las válvulas nativas).
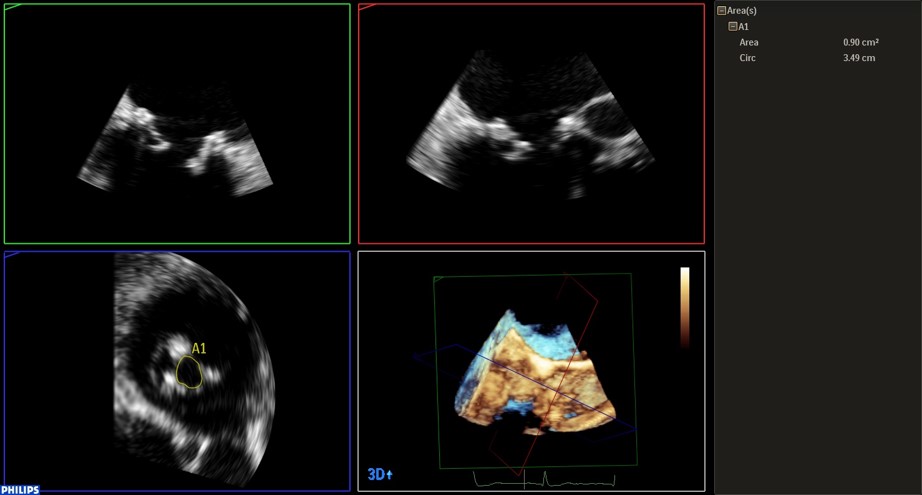
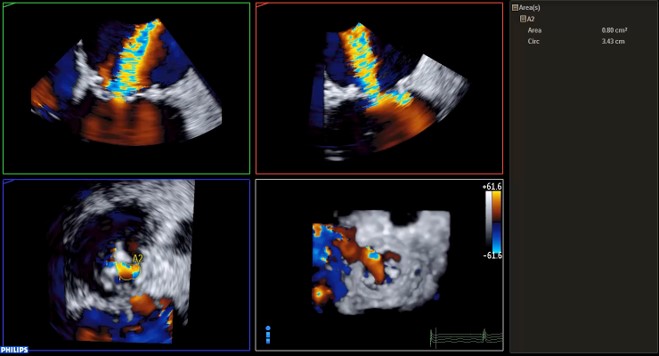
La medición del área de la vena contracta del jet regurgitante central, resulta de 0.8 cm2, compatible con una insuficiencia severa (considerándose severo un valor > 0.4 cm2).
Conclusiones:
• Degeneración estructural precoz de bioprótesis mitral, con gran proliferación fibrocálcica, esclerosis, retracción de velos y perforación de uno de ellos.
• Doble lesión protésica de grado severo.
Nos interesaría conocer su opinión sobre este caso. Lamentablemente no disponemos de suficientes datos clínicos previos a la cirugía ni del postoperatorio inmediato. Consideramos que la elección del tipo de prótesis fue inadecuado en esta paciente.
¿Están de acuerdo con la interpretación diagnóstica?
¿Qué puede explicar una degeneración estructural tan intensa y tan precoz?
Muchas gracias por sus opiniones.
Revisión:
La degeneración valvular estructural (DVE) es un proceso intrínseco e irreversible de la bioprótesis que se manifiesta por cambios degenerativos tales como pannus, fibrosis, calcificación de los velos, delaminación tisular, ruptura y perforación; resultando en disfunción de la misma con caída de su rendimiento hemodinámico, estenosis y regurgitación. Los mecanismos implicados en la DVE no están completamente dilucidados; la evidencia actual sugiere que existen múltiples procesos activos tales como rechazo auto-inmunitario y remodelado tisular de tipo aterogénico.
El inicio de la DVE habitualmente ocurre a partir del 7º – 8º año desde su implantación, siendo máximo a partir de los 10 años.
Uno de los factores determinantes de DVE más importantes es la edad del receptor del injerto, siendo los pacientes más jóvenes los más afectados. Según las recomendaciones actuales se debería optar por una bioprótesis en posición mitral a partir de los 70 años de edad y en posición aórtica a partir de los 65. Otros factores de riesgo para DVE son la HTA, las alteraciones del metabolismo del calcio, la DM, la enfermedad renal avanzada y el mismatch prótesis-paciente.
Los mecanismos fisiopatológicos involucrados en el proceso de DVE protésica no se conocen por completo pero incluyen la disrupción tisular y el engrosamiento y calcificación secundarios al estrés mecánico producidos por el flujo anómalo que opera sobre la superficie de los velos.
La DVE es un proceso continuo, no binario, que se produce a lo largo del tiempo y consta de diferentes estadios de severidad que van desde alteraciones morfológicas de los velos sin compromiso hemodinámico hasta estenosis y/o regurgitación severas.
Lecturas sugeridas:
• Kostyunin A., et al. Degeneration of bioprosthetic heart valves: update 2020. J Am Heart Assoc. 2020. DOI: 10.1161/JAHA.120.018506
• Dvir D., et al. Standardized definition of structural valve degeneration for surgical and transcatheter bioprosthetic aortic valves. Circulation. 2018; 137: 388 – 399. DOI: 10.1161/CIRCULATIONAHA.117.030729
• Vahanian A., et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2021; 00: 1 – 72. DOI:10.1093/eurheartj/ehab395
Continúa la Suscripción de socios SISIAC en sus 3 categorías. Es importante actualizarse como miembro pago para adquirir los beneficios de estar asociado.
Continúa la Suscripción de socios SISIAC en sus 3 categorías.
Es importante actualizarse como miembro pago para adquirir los beneficios de estar asociado.
La cuota anual es de u$s 40 para Socios Adjuntos y u$s 80 para Socios Activos y Fellows.
Si tiene dificultad para realizar el pago, puede consultar el: Instructivo de PayPal.
*80 dólares
*80 dólares
*40 dólares
SOCIOS ACTIVOS, médicos cardiólogos especialistas en imágenes y médicos especialistas en imágenes cardiovasculares de reconocida trayectoria nacional o internacional, que reúnan los créditos necesarios para ello.
Si tiene dificultad para realizar el pago, puede consultar el: Instructivo de PayPal.
Médicos cardiólogos especialistas en imágenes y médicos especialistas en imágenes cardiovasculares.
Antes de cumplimentar el formulario tener preparado en el mismo sistema los siguientes documentos que se solicitarán como obligatorio a adjuntar:
1. Copia del diploma, título, o certificación de su especialización
2. CV actualizado
3. Recomendación de Socio ACTIVO SISIAC
Si tiene dificultad para realizar el pago, puede consultar el: Instructivo de PayPal.
Cardiólogo no especialista en imágenes, clínico, anestesista, terapista, generalista, biólogo, investigador, técnico dedicado a imágenes cardiovasculares, enfermero dedicado a imágenes cardiovasculares u otro profesional con interés en las imágenes cardiovasculares.
Antes de cumplimentar el formulario tener preparado en el mismo sistema los siguientes documentos que se solicitarán como obligatorio a adjuntar:
1. Copia del diploma, título, o certificación de su especialización
2. CV actualizado
Si tiene dificultad para realizar el pago, puede consultar el: Instructivo de PayPal.
Continúa la Suscripción de socios SISIAC en sus 2 categorías Es importante actualizarse como miembro pago para adquirir los beneficios de estar asociado.
La cuota anual es de u$s 40 para Socios Adjuntos y u$s 80 para Socios Activos, Fellows y Socios Asesores.
Beneficios de ser socio de SISIAC pagando una pequeña cuota anual:
Y muchos beneficios adicionales difíciles de cuantificar.... como el ser protagonista junto a muchos imagenólogos que trabajan para superarse y mostrarle al mundo que los latinoamericanos podemos trabajar juntos.
Haga click aquí para informarse de los beneficios y obligaciones de las diferentes categorías de membresía.
Si tiene dificultad para realizar el pago, puede consultar el: Instructivo de PayPal.
"Ser Fellow SISIAC representa uno de los logros más importantes de nuestras vidas académicas. En base a esfuerzo y disciplina hemos alcanzado este mérito, que avala una excelente trayectoria curricular, constituyéndose en un resumen de nuestro trabajo personal, universitario y profesional.
Este reconocimiento reafirma un sentimiento pro-positivo, en la búsqueda y generación de nuevos conocimientos, trabajo en equipo con nuestros colegas connacionales e internacionales, en favor de la educación médica continua, investigación y formación de nuevos médicos cardiólogos y potenciales nuevos Fellows SISIAC.
Agradecemos esta gran distinción que nos honra, y lo dedicamos a nuestras familias, nuestros maestros y a toda la comunidad SISIAC, comprometiéndonos a llevarlo con orgullo y profundo respeto."
PARA ACCEDER A CATEGORÍA FELLOW:
✔ Ser Socio Activo SISIAC con la cuota al día.
✔ Se necesita contar con 1.000 créditos o más, que pueden ser demostrados de diferentes formas.
✔ Descargar esta planilla, donde se encuentran los requisitos y la forma de obtener los créditos.
✔ Enviar a secretaria@sisiac.org la planilla con puntaje discriminado de 1.000 o más créditos, con las constancias correspondientes y el CV, para aprobación del Board Ejecutivo.
*80 dólares
*80 dólares
*40 dólares